|
|
构建能够模拟人体肝脏复杂结构和功能的人工肝组织,一直是再生医学与药物研发领域的重大挑战。现有肝类器官模型普遍存在两大瓶颈:一是难以同时再现肝脏实质细胞、胆管上皮细胞以及功能性微血管系统的时空协调发育;二是大多依赖多能干细胞或多细胞共培养体系,不仅流程复杂、异质性强,且规模化困难。其根本原因在于,传统培养方法无法精准模拟胚胎肝脏发育过程中由黏附信号、机械力与形态发生素共同构成的动态微环境。
2026年4月14日,南开大学生命科学学院张妍与杨军教授团队在《生物技术趋势》上发表题为《Cadherin-engineered microspheres enable scalable biofabrication of multilineage liver organoids》的研究论文。该团队通过将E-钙粘蛋白和VE-钙粘蛋白融合分子修饰到可降解高分子微球表面,并内部封装生长因子,成功构建了一种“智能”生物材料平台。仅需单一来源的间充质干细胞,即可在三维聚集体内自发形成具有血管网络、肝细胞和胆管细胞的多谱系肝类器官。

研究团队首先采用微流控技术制备了直径约22微米的聚乳酸-羟基乙酸共聚物微球,并在其表面稳定修饰E-钙粘蛋白、VE-钙粘蛋白和血管内皮生长因子的融合蛋白,同时内部封装成纤维细胞生长因子和肝细胞生长因子。当将人间充质干细胞与这些功能化微球按3:1比例混合离心后,细胞与微球快速自组装成致密的杂合聚集体。实验发现,E-钙粘蛋白通过同亲性相互作用增强了细胞间连接,激活了α-连环蛋白/肌动蛋白骨架/机械敏感转录共激活因子信号轴,促进细胞核内YAP聚集,并上调多能性相关基因表达。这一过程不仅显著增强了细胞聚集体内的机械传导,还诱导了抗凋亡信号通路活化,为干细胞后续的定向分化奠定了“可塑性”基础。
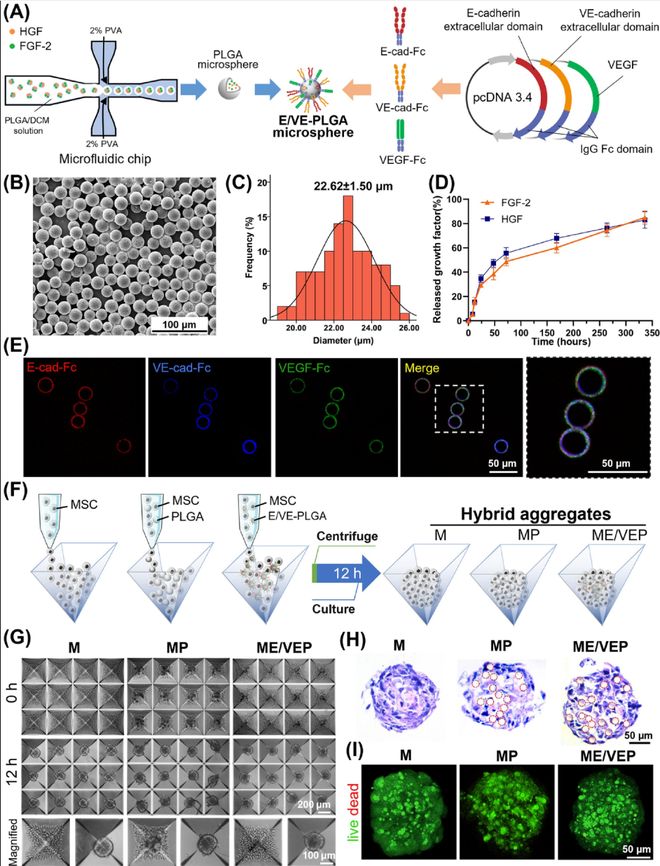
在进入肝-内皮诱导分化阶段后,VE-钙粘蛋白与血管内皮生长因子的协同作用展现出关键功能——它们引导间充质干细胞在聚集体内部形成内皮细胞核心。这些新生内皮细胞并非被动填充,而是主动分泌转化生长因子-β并激活NOTCH信号通路,且这两种发育信号的活化强度从聚集体核心向外周呈梯度衰减。单细胞转录组测序进一步揭示,高表达NOTCH2的胆管细胞样群体显著富集了ONECUT2、CLDN4等胆管特异性基因;同时,成纤维细胞生长因子2与CD44的配体-受体对与肝细胞分化标志物呈正相关。通过配体-受体网络分析,研究团队还鉴定出间充质细胞通过多种信号通路与肝细胞、胆管细胞及内皮细胞形成的复杂通讯图谱。经过14天至4周的培养,这些类器官自发分化为清淅分区的肝细胞(表达白蛋白、HNF4A)、胆管细胞(表达CK19)、内皮细胞(表达CD31)及间充质细胞,并展现出成熟肝细胞功能——白蛋白分泌量达2微克/百万细胞/天,尿素合成约20微克/百万细胞/天,约为原代人肝细胞水平的55%。在对乙酰氨基酚和异烟肼的毒性测试中,该类器官呈现典型的剂量依赖性损伤反应,包括线粒体活性氧升高、磷酸化JNK上调及线粒体DNA释放至胞浆,与临床肝损伤特征高度一致。该平台为药物筛选、疾病建模乃至再生医学提供了一种可规模化、可复制的工程化策略。
READING
BioPeers
欢迎关注本公众号,所有内容欢迎点赞,推荐❤️,评论,转发~
如有错误、遗漏、侵权或商务合作请私信小编~~
欢迎大家投稿课题组 研究进展 、招聘及招生宣传~
所有文章只为科普、科研服务,无商业目的~ |
|